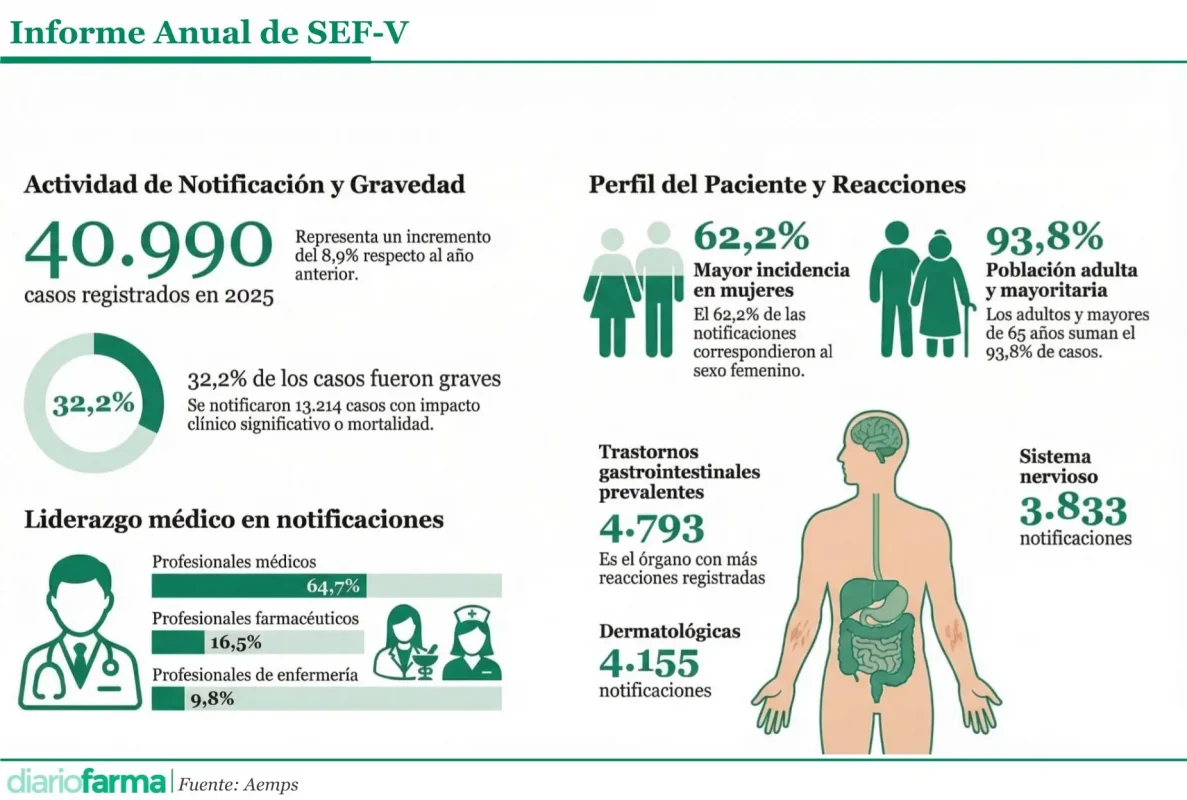
El ‘Informe Anual del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano’ de 2025 recoge una tendencia ascendente en la actividad del sistema, con un total de 40.990 notificaciones de sospechas de reacciones adversas (RAM). Esta cifra representa un incremento del 8,9 por ciento respecto al año anterior, consolidando una tasa de notificación global de 41 casos por cada 100.000 habitantes.
Según los datos del estudio publicado por la Agencia Española de Medicamentos y Productos Sanitarios (Aemps), del volumen total de comunicaciones registradas, el 48,7 por ciento se remitió de forma directa al SEFV-H, mientras que el 32,2 por ciento de las sospechas fueron clasificadas como graves. En cuanto al perfil clínico de las notificaciones, la tipología de los incidentes guardó sintonía con periodos previos. Los trastornos gastrointestinales, los de la piel y el tejido subcutáneo, y aquellos relacionados con el sistema nervioso central destacaron como las áreas con mayor incidencia en los reportes recibidos.
Herramientas para la seguridad clínica
Durante el pasado año, el sistema, que integran los centros autonómicos bajo la coordinación de la Aemps, centró sus esfuerzos en el refuerzo técnico y metodológico de la vigilancia. En este sentido, la agencia ha difundió tres documentos de carácter estratégico. El primero de ellos, el ‘manual de uso de www.notificaRAM.es’, se diseñó como una guía práctica para facilitar el uso del formulario electrónico tanto a los profesionales sanitarios como a los ciudadanos.
A esta herramienta se sumó la ‘guía de codificación del SEFV-H’, orientada a unificar los criterios de registro de los casos detectados. Según detalla el informe, este documento abordó aspectos técnicos que solían generar dudas entre los evaluadores, con el objetivo de establecer un consenso que facilite el análisis posterior de las notificaciones. La homogeneidad en la codificación resulta crítica para garantizar la calidad del dato primario en el sistema de vigilancia nacional.
Metodología en detección de señales
El bloque normativo del ejercicio se completó con la ‘guía para la detección de señales del SEFV-H’. Este texto describe los procedimientos utilizados por los técnicos para identificar potenciales nuevos riesgos o variaciones en la seguridad de fármacos ya autorizados. La detección de estas señales se define en el informe como el paso previo indispensable para la toma de decisiones reguladoras que protejan la salud pública.
La publicación de estos manuales quiere fomentar la notificación activa y compartir criterios técnicos de interés para la evaluación de riesgos. Desde la Aemps se agradece la colaboración de los profesionales y la población, al tiempo que se recordó la importancia de comunicar cualquier sospecha para identificar cambios en el perfil de seguridad de los medicamentos de uso humano. En palabras de la agencia, 'tu notificación importa', para reforzar la vigilancia continua de los tratamientos en el mercado.






 Lilisbeth Perestelo:
Lilisbeth Perestelo:  César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):