Nicolás González Casares propone facilitar el intercambio de terapias avanzadas desarrolladas bajo el régimen de exención hospitalaria entre Estados miembros. Así se recoge en el informe elaborado por el eurodiputado socialista, como ponente designado en la Comisión de Salud Pública (SANT) del Parlamento Europeo, sobre el futuro Plan de Acción Europeo sobre Enfermedades Raras, al que ha tenido acceso Diariofarma.
El documento propone explorar un marco que permita compartir estos tratamientos en determinadas circunstancias, especialmente cuando los pacientes no puedan desplazarse o cuando el número de afectados sea extremadamente reducido.
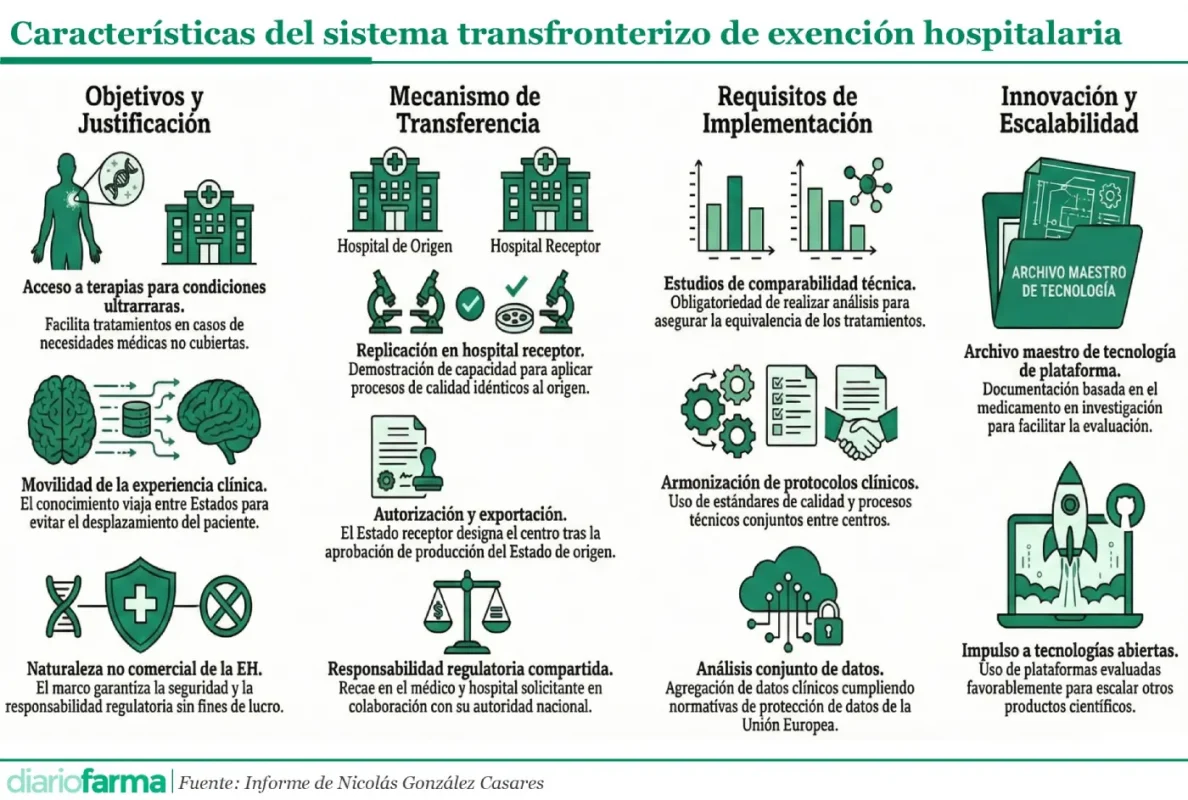
La propuesta se incluye dentro del capítulo dedicado al acceso a tratamientos y terapias avanzadas en el futuro marco europeo sobre enfermedades raras que el informe sugiere desarrollar. El texto parte de constar que muchas de estas patologías afectan a poblaciones muy pequeñas y dispersas, lo que limita la capacidad de los sistemas sanitarios nacionales para desarrollar y aplicar terapias innovadoras de forma aislada. En ese contexto, plantea reforzar la cooperación transfronteriza para aprovechar la experiencia acumulada en determinados centros especializados.
Entre las recomendaciones incluidas en el informe figura la posibilidad de establecer un esquema de intercambio transfronterizo de medicamentos de terapias avanzadas desarrollados bajo el régimen de exención hospitalaria, con el objetivo de facilitar el acceso de pacientes a tratamientos innovadores que se hayan desarrollado en hospitales de otros Estados miembros.
La exención hospitalaria es una figura prevista en la legislación farmacéutica europea que permite utilizar medicamentos de terapias avanzadas sin autorización centralizada de comercialización cuando se producen de forma no rutinaria, bajo responsabilidad médica y para un paciente concreto en un hospital autorizado. Hasta ahora, su aplicación ha estado fundamentalmente vinculada al ámbito nacional, lo que ha limitado la posibilidad de que tratamientos desarrollados en centros concretos puedan aplicarse en otros países.
El informe sugiere que, en determinados supuestos, estos tratamientos puedan transferirse entre Estados miembros. Entre las situaciones contempladas se encuentran aquellas en las que el estado clínico del paciente impida su desplazamiento al país donde se ha desarrollado la terapia o cuando el número de pacientes en el Estado receptor sea demasiado reducido para justificar la creación de una capacidad propia de producción.
Según el esquema planteado, el hospital del país receptor podría solicitar una autorización de exención hospitalaria ante su autoridad nacional, siempre que pueda demostrar su capacidad para aplicar el tratamiento siguiendo los mismos estándares de calidad, seguridad y proceso que el centro que lo desarrolló inicialmente. El modelo permitiría incluso que parte de las actividades de fabricación continuaran realizándose en el país de origen, siempre que se mantenga la coherencia con el proceso productivo original.
El texto subraya que este tipo de cooperación debería apoyarse en protocolos clínicos y de calidad armonizados, así como en la realización de estudios de comparabilidad que garanticen que el tratamiento mantiene los mismos estándares científicos y regulatorios. Asimismo, plantea la necesidad de agregar y analizar conjuntamente los datos clínicos generados en los distintos centros implicados, respetando la normativa europea de protección de datos.
Con esta aproximación, el informe apunta a una interpretación más flexible del régimen de exención hospitalaria, orientada a aprovechar el conocimiento acumulado en determinados centros especializados y a facilitar el acceso a terapias avanzadas en enfermedades con poblaciones extremadamente reducidas. El planteamiento se alinea además con el funcionamiento de las Redes Europeas de Referencia, que buscan concentrar conocimiento clínico en nodos europeos para enfermedades complejas o poco frecuentes.
Acceso a terapias y financiación pública
El informe también introduce otras recomendaciones orientadas a mejorar la disponibilidad de tratamientos innovadores para enfermedades raras. Entre ellas figura la posibilidad de vincular determinadas ayudas europeas a compromisos de accesibilidad cuando el desarrollo de terapias avanzadas haya recibido financiación pública.
En concreto, el texto plantea que cuando proyectos financiados con fondos de la Unión contribuyan al desarrollo de medicamentos destinados a estas patologías, los beneficiarios deberán garantizar que la explotación de los resultados contribuya a su disponibilidad y asequibilidad en los Estados miembros. Para ello, los acuerdos de financiación podrían incluir obligaciones adicionales, como la elaboración de planes de acceso que definan estrategias y plazos para facilitar la llegada de los tratamientos a los pacientes.
El informe sugiere además promover la creación de plataformas tecnológicas abiertas para el desarrollo de terapias avanzadas. Estas plataformas permitirían poner a disposición de terceros determinados datos regulatorios y componentes científicos validados bajo condiciones transparentes y no discriminatorias, con el objetivo de facilitar el desarrollo de nuevos productos basados en la misma tecnología.
Este enfoque pretende reducir costes y acelerar el desarrollo de terapias en enfermedades con poblaciones muy reducidas, donde la repetición de procesos regulatorios y científicos puede convertirse en un obstáculo significativo.
Cooperación europea en acceso
Las recomendaciones incluidas en el informe también apuntan a reforzar la cooperación entre Estados miembros en la generación de evidencia clínica y en la evaluación de tratamientos, con el objetivo de reducir las desigualdades en disponibilidad de terapias para enfermedades raras en la Unión Europea.
En este sentido, el documento menciona la posibilidad de avanzar en mecanismos de cooperación voluntaria, incluidos esquemas de generación conjunta de evidencia clínica o iniciativas de compra conjunta cuando resulte adecuado.
Todas estas propuestas forman parte de las recomendaciones que el Parlamento Europeo plantea trasladar a la Comisión para el desarrollo de un futuro marco europeo en enfermedades raras. El informe deberá ahora iniciar su tramitación en la comisión parlamentaria SANT.








 Lilisbeth Perestelo:
Lilisbeth Perestelo:  César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):