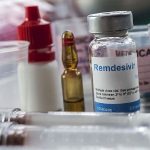
Gilead ha informado de una solicitud remitida a la Agencia Americana de Medicamentos (FDA), para desistir de la designación huérfana concedida al antiviral que actualmente se encuentra en investigación para el Covid-19, remdesivir, renunciando así a todos los beneficios derivados de dicha designación, desde la confianza en que podrá conseguir igualmente una revisión "expeditiva" para su producto.
"Contactos recientes con las agencias regulatorias nos muestran que la solicitud y la revisión del dossier de remdesivir como tratamiento del Covid-19 está siendo ágil. A comienzos de marzo, se nos concedió designación huérfana, aunque esta suele darse a tratamientos que afectan a menos de 200.000 pacientes en Estados Unidos", precisan.
Recuerdan que entre los beneficios de la desinación huérfana está la exención de la obligación de presentar un plan de investigación sobre su uso pediátrico previo a la solicitud de autorización, un proceso que suele llevar, según el laboratorio, más de 210 días.
Gilead concluye su comunicado reconociendo la urgencia pública por el Covid-19 y asegura que está trabajando para avanzar en el desarrollo del fármaco para que esté disponible lo antes posible, del cual irá informando a medida que se vayan generando resultados.















 Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia:  Carmen Martínez, portavoz del Grupo Socialista en la Comisión de Sanidad del Congreso de los Diputados:
Carmen Martínez, portavoz del Grupo Socialista en la Comisión de Sanidad del Congreso de los Diputados: