A finales de 2022, un total de 60 medicamentos huérfanos permanecen sin financiar en España. Son cinco más que los que se registraron en 2021 y casi la mitad de ellos llevan esperando financiación del Sistema Nacional de Salud más de tres años. Estas son algunas de las conclusiones a las que la Asociación Española de Laboratorios de Medicamentos Huérfanos y Ultrahuérfanos (Aelmhu) ha llegado, de acuerdo con los resultados preliminares de su Informe de Acceso 2022.
A la vista de estos datos, María José Sánchez Losada, presidenta de Aelmhu, considera que es necesario “reivindicar, una vez más, que España debería ser capaz de simplificar los procesos de aprobación de MM.HH. a nivel nacional, sobre todo porque su eficacia ya ha sido acreditada por la Agencia Europea del Medicamento (EMA)”.
La asociación considera que, a nivel comunitario, el año pasado fue “excelente” ya que registró “máximos históricos en designaciones huérfanas de productos con nombre comercial, con un total de 29; así como de autorizaciones de comercialización europeas (24). Esto hace que el número de medicamentos huérfanos autorizados en Europa alcance en la actualidad los 146.
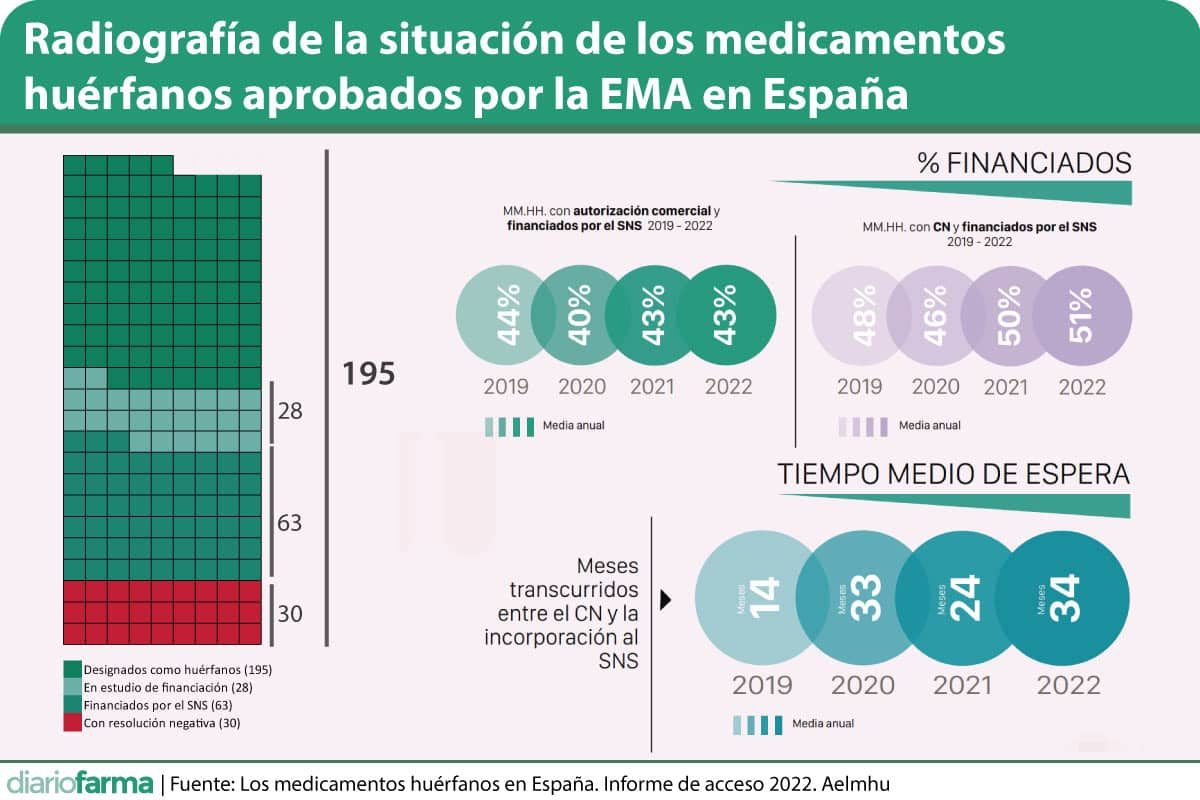
Por el contrario, si nos fijamos en España, el estudio revela que los indicadores nacionales “se encuentran lejos de ser extraordinarios”, explica Aelmhu. La asociación reconoce que, si bien 17 nuevos medicamentos huérfanos. adquirieron código nacional (CN) en nuestro país, solo nueve fueron financiados, lo que representa un descenso de un 37% con respecto al ejercicio pasado (cinco productos financiados menos). Además, el 100% de esos nuevos productos financiados obtuvieron un precio condicionado: todos presentan condiciones de seguimiento, cuatro están sometidos a coste máximo por paciente y dos tienen techo de gasto.
En total, a 31 de diciembre de 2022, España contaba con 123 medicamentos huérfanos. con CN y 63 financiados, lo que significa que 23 aprobados a nivel europeo no han llegado todavía a nuestro mercado, el 16% del total de los autorizados a nivel comunitario, la cifra más alta de los últimos cuatro años.
Uno de los elementos que más influye en esta situación son los dilatados tiempos de espera que, lejos de mejorar, aumentaron un 42% en el último ejercicio. Así, el tiempo promedio entre el CN y la financiación de un producto huérfano supera en nuestro país los 34 meses, casi tres años, muy lejos de los seis meses deseables como tiempo medio máximo para la aprobación y financiación.















 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: 