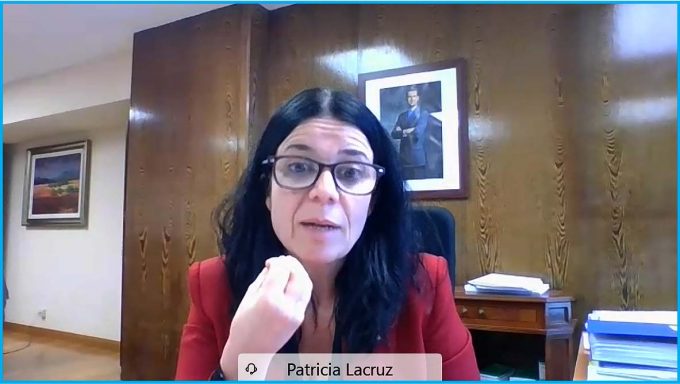
Pese a la pandemia de la covid-19, que ha marcado de forma casi exclusiva la actividad del Ministerio de Sanidad y en gran parte de la Dirección General de Cartera Común de Servicios del SNS y Farmacia, la realidad es que el trabajo de esta entidad no se ha parado a lo largo de los últimos meses en lo referido a los planes que ya tenían en marcha. Por ello, muchos de ellos están ya ultimándose para ser puestos en marcha en los últimos meses. Para profundizar sobre ellos, Diariofarma ha entrevistado a Patricia Lacruz de cara a conocer algunos detalles más de lo conocido hasta el momento.
Pregunta. Hace unos días presentó las líneas generales del ‘Plan para la consolidación de los informes de posicionamiento terapéutico (IPT) de los medicamentos en el Sistema Nacional de Salud (SNS)’ y aunque fue extensa la presentación y ya está disponible el plan, hay algunas cuestiones en las que querríamos profundizar. Aunque ahora mismo el Plan no lo contempla, ¿sería posible que, de acuerdo con la visión de su IPT ideal que planteó el Comité Asesor de la Prestación Farmacéutica (CAPF), las compañías presenten sus evaluaciones de acuerdo con los criterios establecidos por la administración?
Respuesta. Actualmente, en el procedimiento de financiación y precio, los titulares deben aportar una serie de documentación a través de Gesfarma en materia de costes e impacto presupuestario. Nuestro objetivo es utilizar esta estructura, aunque queremos mejorarla, no solo en el marco de la presentación de ofertas para la fijación de precio sino también para la etapa previa. Estamos trabajando con la AIReF para generar una guía metodológica para la presentación de la información para que sea lo más efectiva posible para el análisis posterior de la evaluación económica. Espero que se pueda poner en marcha en el primer trimestre de 2021.
P. ¿Pero no se plantean pedir a la industria que presente sus estudios de coste-efectividad?
R. La información que nos presenta la compañía en el dosier de valor del expediente ya incluye tanto costes como impacto presupuestario y también información relativa a modelos económicos. Esta información ya la presenta aquel que quiere. Lo que sí tenemos definida es una metodología para hacer la evaluación en la Dirección General y en el marco de la red. La evaluación económica no es algo nuevo para el sistema, lo hacemos día a día el equipo de evaluación de la Dirección General.
P. ¿Y qué precios se van a elegir para esa fase previa?
R. Va a depender de la evidencia disponible y de si hay o no comparadores. En función de eso se hará una estimación. Los precios, que se adaptarán en función de los comparadores, serán costes de adquisición y en ningún momento se trasladarán en formato monetario, sino en unidades equivalentes. Se tomará como unidad la que tenga un coste menor y en función de las distintas alternativas se hará la correspondiente equivalencia con ese precio unitario.
“[El ‘manifiesto de los 300’] es una iniciativa positiva porque pone de relieve la importancia de la evaluación en las políticas públicas sanitarias”
“Tengo que decir que en el manifiesto se traslada que hay una arbitrariedad en la toma de decisiones de inclusión en cartera de algún medicamento. Quiero ser muy clara y contundente: Esa arbitrariedad no existe”
“Tenemos agencias integradas en la RedETS con mayor antigüedad que el propio NICE y que la producción científica de la Red es superior a la del organismo inglés”
P. Esas unidades equivalentes son solo en función de los comparadores directos...
R. Efectivamente.
P. Entonces, no se va a desvelar el precio de adquisición, ¿se va a proteger?
R. Yo no hablaría de protección. El precio de adquisición es cambiante en función de las distintas ofertas que se pueden producir en el ámbito de la competencia, hablando de medicamentos del ámbito hospitalario, por lo que creo que lo más efectivo es hablar de equivalencias. Esto nos permitirá que las evaluaciones tengan una vigencia mucho mayor en el tiempo, incluso con cambios de los costes de adquisición.
P. Entonces, el resultado de la evaluación no será tantos euros por AVAC, sino tantas unidades equivalentes por AVAC…
R. Lo que pretendemos es que, en materia de precios estimados o costes, hablemos de unidades equivalentes, que es lo que puede permitir visibilizar mejor la lectura y tendrá más duración.
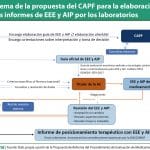
P. ¿Habrá algún tipo de garantía de cumplimiento de los plazos para completar los IPT?
R. Hemos desarrollado un cuadro de mando que nos ayudará a monitorizar el cumplimiento de los plazos. El plazo comienza a contar en el momento en que se asigna el IPT al equipo evaluador correspondiente, que es el de la evaluación terapéutica. Esta asignación tiene lugar cuando el laboratorio ha mostrado su interés en la comercialización del producto y tras la priorización de los IPT previos. Nuestro objetivo es llegar a los 90 días tras la asignación. Para intentar hacerlo posible hemos invertido en infraestructura y diseñado una metodología clara, además de la monitorización.
P. Esta misma semana Facme ha mostrado sus dudas acerca de la composición de los nodos y la falta de transparencia en relación con sus componentes. ¿Será pública?
R. Lo primero que quiero dejar claro es que, en la red, tal y como está conformada, forman parte más de 15 especialidades tanto médicas como farmacéuticas. Los expertos tienen una participación activa en los nodos, que están formados por coordinadores, co-coordinadores y miembros. Las comunidades autónomas nombran los miembros de forma directa y los coordinadores y co-coordinadores por la Comisión Permanente de Farmacia. En cualquier caso, lo que se puede ver es solo una parte de la red. Hay comunidades autónomas que han propuesto a expertos clínicos en evaluación para los distintos nodos, mientras que otras han designado a profesionales en gestión y coordinación porque tienen su propia red de evaluación. De este modo, si digo que hay 15 especialidades y 120 expertos, me quedo corta ya que la estructura es capilar, de acuerdo con el funcionamiento de su red de evaluación.
P. ¿Pero se harán públicos los nombres de los profesionales que participen?
R. Eso será una decisión personal de cada persona que participa en la red. A mi no me cabe la menor duda de que todos los profesionales del SNS son excelentes en el marco de sus actividades.
P. ¿Igual para el grupo coordinador?
R. Sí.
P. Otro aspecto que siempre ha preocupado en el tema de los IPT es su revisión, tal vez porque había pocos recursos. ¿Será posible asegurar la revisión de los IPT cuando aparezca nueva evidencia?
R. Actualmente los IPT se revisan cuando hay evidencia científica publicada. A partir de ahora se seguirá igual. Por ejemplo, si hay una autorización condicional y se completa un ensayo clínico, se publican resultados y hay nueva evidencia y se podrá revisar. Si se modifica el posicionamiento, el procedimiento seguirá el diagrama de flujo.
P. ¿Y se podrá solicitar la revisión a instancia de parte?
R. Esto no es un procedimiento administrativo. Aquí los laboratorios pueden presentar información relacionada con su producto mientras que esté el procedimiento abierto o si hay una nueva evidencia. Pero he de decir que las personas que forman parte del grupo de coordinación, también el de antes, disponen de esa información y en caso necesario se plantea. Queremos que el IPT esté actualizado para la toma de decisiones.
P. Me refiero más a casos en los que hay un IPT con más de 5-6 años y que ha quedado obsoleto. ¿En ese caso se podría decir por parte de profesionales o la industria que se revise?
R. Si hay evidencia publicada que indique que haya que proceder a la revisión, se hará. Si es información que responda a evidencia sin una metodología clara, no procederá la revisión. Se hará según el sentido común.
P. Le pongo el ejemplo de los ACOD, que las sociedades científicas indican que el IPT está obsoleto
R. Ese IPT ya se está revisando. Se inició en época prepandemia…
P. Parece que hay profesionales que no lo saben…
R. Yo misma trasladé a las sociedades científicas nuestro compromiso de revisión de este IPT.
P. Este lunes se ha hecho público un manifiesto de 300 expertos pidiendo la creación de una agencia tipo AIReF pero de evaluación económica. ¿Cómo lo valora?
R. Es una iniciativa positiva porque pone de relieve la importancia de la evaluación en las políticas públicas sanitarias. También te digo que en el marco de las distintas acciones que hemos emprendido en el Ministerio, hay una apuesta clara en la evaluación: empezamos con Valtermed, seguimos con RevalMed, el fortalecimiento de la Red de Agencias Evaluación de Tecnología Sanitaria (RedETS), a la que hemos duplicado el presupuesto en 2021, y ahora incorporamos en el Proyecto de Ley de Medidas de Equidad, Universalidad y Cohesión, que pretende que el enfoque de salud en todas las políticas sea una acción de gobierno y que todas las normas tengan una evaluación de impacto en salud. Son cuatro ejemplos que muestran que la evaluación es una apuesta firma del gobierno.
“Los precios, que se adaptarán en función de los comparadores, serán costes de adquisición y en ningún momento se trasladarán en formato monetario, sino en unidades equivalentes”
“Cuando digo que hay 15 especialidades y 120 expertos [en RevalMed], me quedo corta ya que la estructura es capilar, de acuerdo con el funcionamiento de su red de evaluación”
P. Y sobre el manifiesto en sí…
R. Tengo que decir que en el manifiesto se traslada que hay una arbitrariedad en la toma de decisiones de inclusión en cartera de algún medicamento. Quiero ser muy clara y contundente: Esa arbitrariedad no existe. En el SNS hay una red de Agencias de Evaluación de Tecnologías y, por otro, una Dirección General, cuyos informes son preceptivos para la toma de decisiones. Posteriormente, los informes se someten a los órganos colegiados que deciden y en función de los mismos se toman las decisiones. No hay ninguna decisión que se tome de forma arbitraria de cara a incluir en la cartera del SNS una prestación, medicamento o tecnología.
P. El manifiesto también pone énfasis en la independencia…
R. Yo no conozco profesionales más independientes que los funcionarios y funcionarias de la Administración Sanitaria y no creo que haya una mayor independencia financiera que la que otorgue unos presupuestos públicos. También quiero decir que, aunque hace tiempo que se habla del HispaNICE, tenemos agencias integradas en la RedETS con mayor antigüedad que el propio NICE y que la producción científica de la Red es superior a la del organismo inglés. Igualmente, quiero hacer referencia a que las agencias de evaluación tienen una representación internacional muy relevante, quizá más que la que se conoce. Además, la RedETS es un ejemplo de cohesión y, aunque siempre hay que mejorar, y aprender de quienes lo hacen mejor, pero también tenemos que poner en valor lo que tenemos en el sistema y visibilizarlo y en ello estamos trabajando.

P. Entre los firmantes del acuerdo hay expertos en gestión, conocedores de la función pública, y a pesar de ello proponen ese organismo, por lo que no lo hacen desde el desconocimiento…
R. Solo conocemos el texto del manifiesto publicado en los medios ya que no han contactado previamente con nosotros y no sé si han solicitado ya la reunión para abordar este tema. Lo que veo es un texto en el que estoy conforme en la apuesta por la evaluación, pero lo que quiero destacar es lo que sé de primera mano qué se hace en el Sistema Nacional de Salud. Esa frase de la arbitrariedad del procedimiento me hace pensar que o bien no se conoce el procedimiento o bien las estructuras actuales del SNS para ello, más allá de que sean mejorables. Por eso quiero insistir en que ninguna de las decisiones es arbitraria y que hay estructuras en marcha y otras que se están poniendo ahora para cumplir con esos objetivos que plantea el manifiesto. Valtermed hace un año y un mes que se puso en marcha. Hay convencimiento firme de que la evaluación es esencial para la toma de decisiones.














 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: 