
Como en años anteriores, desde Simon-Kucher hemos analizado las tendencias en financiación de medicamentos en España a lo largo de este pasado 2025. Con el fin de entender cómo éstas han evolucionado con respecto a los años anteriores, hemos estudiado las principales fuentes que recogen las resoluciones de financiación de medicamentos: las notas informativas de la Comisión Interministerial de Precios de Medicamentos (CIPM) y el buscador de la información sobre la situación de financiación de los medicamentos (Bifimed), y hemos dado respuesta a las siguientes preguntas: ¿cuál es la distribución de acuerdos positivos de precio y financiación frente a los acuerdos denegatorios? ¿Qué porcentaje de decisiones de financiación positivas se tomaron en la primera reunión de la CIPM y cómo ha evolucionado el tiempo requerido para alcanzar un acuerdo de financiación? ¿Cuáles son las condiciones especiales de financiación más recurrentes y cómo difiere de lo observado en años anteriores?
Durante el año 2025, en el transcurso de 11 reuniones de la CIPM, se han formalizado un total de 180 acuerdos de financiación, abarcando como es habitual tanto decisiones positivas como denegatorias. Esta cifra es ligeramente inferior a la del año anterior donde se establecieron 185 acuerdos. Al igual que en los estudios publicados previamente, este análisis se enfoca únicamente en medicamentos con nuevos principios activos o combinaciones, así como nuevas indicaciones de medicamentos ya incluidos en la prestación farmacéutica del Sistema Nacional de Salud (SNS)1. Asimismo, han sido excluidos aquellos acuerdos referentes a las alteraciones en la oferta, y los aplicables a vacunas, medicamentos genéricos/biosimilares y dispositivos médicos2.
En este último año, la proporción de decisiones de financiación positivas frente a negativas se ha mantenido generalmente estable frente a 2024 y los años anteriores. Concretamente, en 2025, el 50% (90) de los expedientes negociados con la Subdirección General de Farmacia (SGF) obtuvieron una decisión positiva de financiación, al igual que en 2024, donde el 51% de acuerdos fueron de carácter positivo.
Asimismo, se sigue apreciando una mayor agilidad en la toma de decisiones de financiación. En 2025, aproximadamente el 70% de los acuerdos positivos (63/90) se han dado en una primera reunión de la CIPM, en línea con lo observado durante 2024.
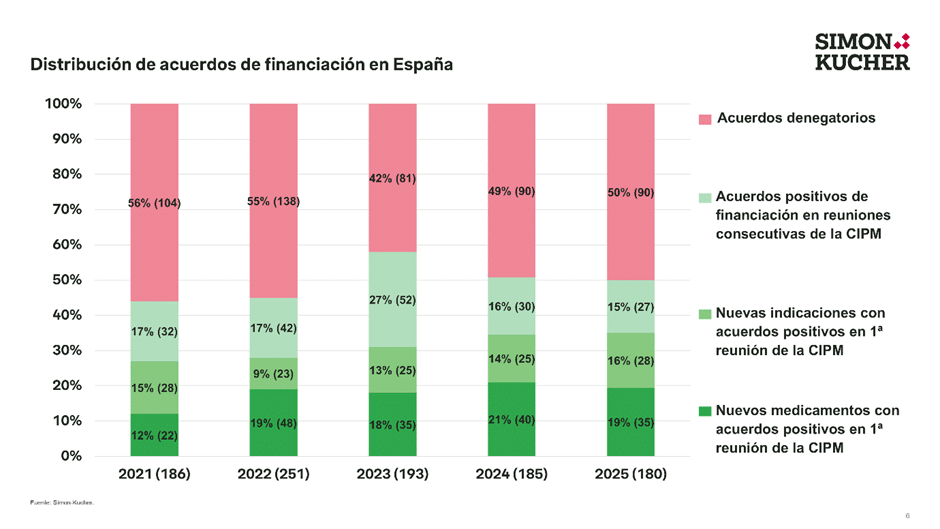
(*) Los acuerdos positivos de financiación pueden incluir varias indicaciones para un único producto en el caso de haber sido resueltos simultáneamente en la misma reunión de la CIPM.
En relación con las decisiones positivas que precisaron de más de una reunión de la CIPM, se ha observado que, tras una primera denegación, la media de tiempo hasta la aprobación fue de aproximadamente 225 días y la mediana fue de 140 días, dado que en 2025 se ha dado resolución a ocho procesos que llevaban más de un año pendientes de decisión (el periodo más corto fue de 56 días y el más largo de 791). Se observa una clara reducción a lo largo de los años, con las medianas en 2024 y 2023 siendo 182 días y 224 días respectivamente.
Enfocándonos exclusivamente en los acuerdos de financiación positivos, este análisis tiene como objetivo, una vez más, entender las tendencias en condiciones especiales de financiación implementadas a lo largo del año 2025 y cómo difieren con respecto a lo observado en los cuatro años anteriores.
De forma general, las condiciones especiales de financiación se pueden agrupar en tres categorías: (1) Condiciones relacionadas con medidas del control del gasto, (2) Condiciones que implican una restricción en la indicación o acceso al tratamiento y (3) Acuerdos especiales de financiación.
1.- Condiciones relacionadas con medidas del control del gasto:
La racionalización del gasto público y el impacto presupuestario continúan siendo criterios clave en la financiación de un medicamento, por lo que las medidas del control del gasto han vuelto a ser ampliamente utilizadas. Al igual que en los últimos años, en 2025, casi el 100% de los acuerdos positivos llevan asociada alguna de estas medidas. Entre ellas, las más comunes siguen siendo la revisión anual de ventas y del precio fijado. En 2025, estas medidas han sido aplicadas en el 95% (86) de los acuerdos positivos, por encima del 86% observado en 2024, y han quedado en varios casos reflejadas en Bifimed como un umbral de ventas. Por último, también se ha observado el establecimiento de reservas singulares en el 40% de los casos, consistente en controlar y limitar la dispensación de un medicamento, sin necesidad de visado, a los pacientes no hospitalizados en los Servicios de Farmacia hospitalarios.
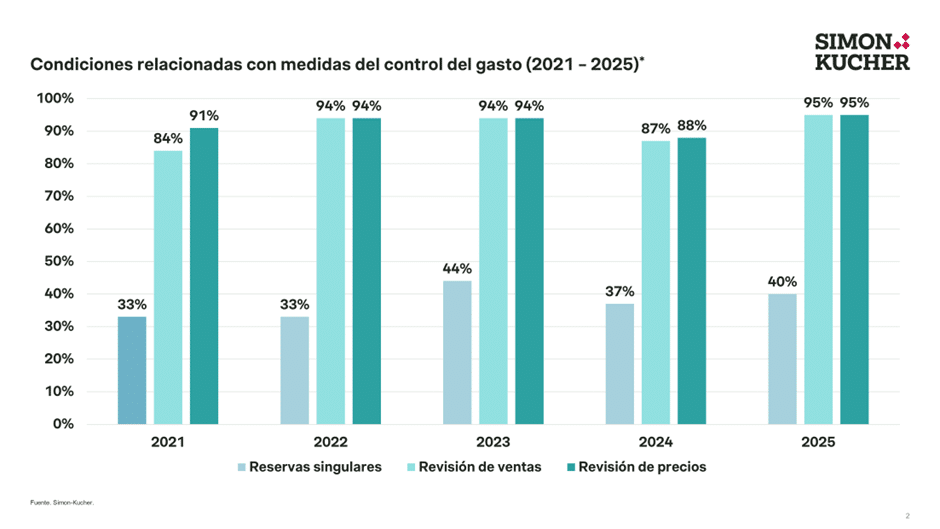
(*) El porcentaje de medidas de control del gasto se ha calculado de forma individual para cada una de las medidas, siendo común que los acuerdos de precio y financiación conlleven más de una medida de control del gasto. Es por esto, que la suma de los porcentajes no equivale a 100% dentro de cada año.
2.- Condiciones que implican una restricción en la indicación o acceso al tratamiento
La implementación de restricciones de financiación con respecto a la indicación aprobada por la Agencia Europea del Medicamento (EMA) continúa siendo frecuente en 2025. Se ha mantenido generalmente estable a lo largo de los cinco años analizados para productos hospitalarios o dispensados en farmacia hospitalaria, estando un 42% (31) de los acuerdos la financiación sujetos a este tipo de condición. En cuanto a los acuerdos referentes a medicamentos dispensados en farmacia comunitaria, se observa más variabilidad a lo lago de los años. En 2025 concretamente, se ha incorporado un visado de inspección en el 19% (3) de los medicamentos, incluyendo restricciones adicionales en su acceso.
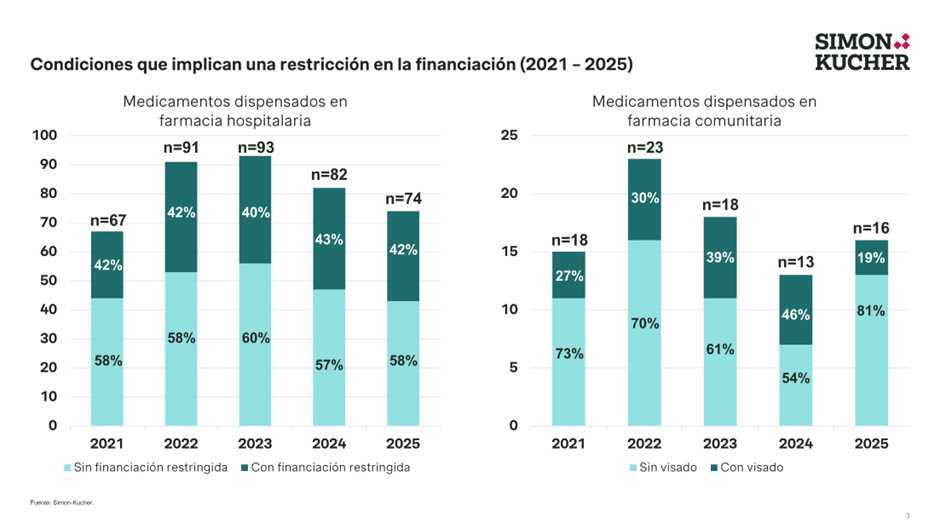
(*) Durante el año 2025 y para la muestra evaluada3, un 82% de los acuerdos positivos (74) fueron sobre fármacos hospitalarios o dispensados en farmacia hospitalaria, en línea con 2024, donde este porcentaje fue casi del 86% (82).
3.- Acuerdos especiales de financiación
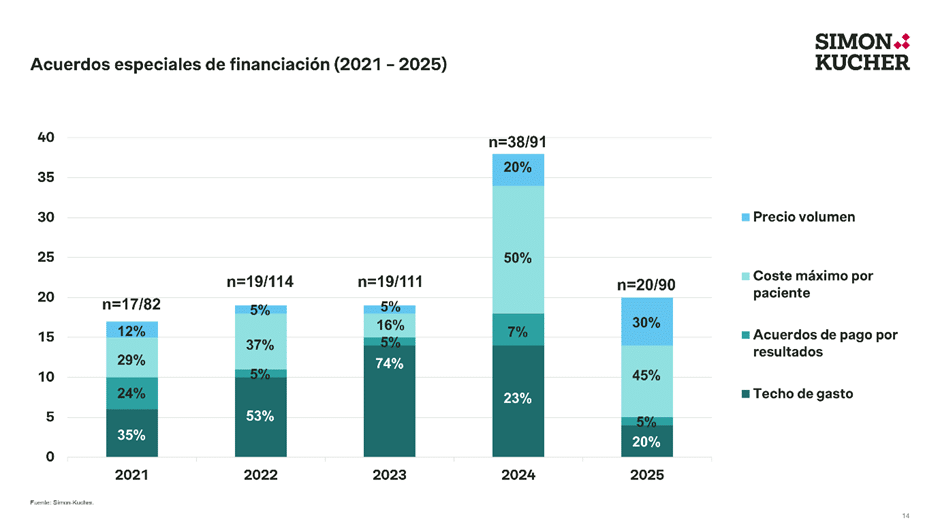
De las decisiones positivas de financiación analizadas en 2025 (90), un 22% (20) está sujeto a algún tipo de acuerdo especial de financiación, una disminución notable frente al 32% (30) observado en 2024, pero en línea con los años anteriores.
Se mantiene una marcada tendencia hacia la negociación de acuerdos puramente financieros. En este último año, los acuerdos de coste máximo por paciente se han mantenido como acuerdo principal, con 9 (45%) negociados, sin embargo, la implementación de techos de gasto ha disminuido sustancialmente, 4 (20%), frente a los años anteriores. Asimismo, en 2025 se han establecido 6 (30%) acuerdos de precio / volumen y 1 (5%) acuerdo de pago por resultados (en base a las fuentes disponibles).
Se observa que los acuerdos especiales de financiación se siguen utilizando como herramienta clave para productos de alto impacto presupuestario o que generan gran incertidumbre presupuestaria. Además, durante este último año, 18 de los acuerdos especiales de financiación, un 90% del total, han sido publicados para nuevos medicamentos, y únicamente 2 nuevos acuerdos para nuevas indicaciones de medicamentos previamente financiados. Existen también, más allá de estos acuerdos especiales de financiación, medidas complementarias como suministros de prueba diagnóstica sin coste o descuentos adicionales que pueden verse reflejadas para ciertos productos en Bifimed.
Entonces, ¿cómo han evolucionado las tendencias en financiación de medicamentos en España durante 2025 respecto a los cuatro años anteriores?
- Se observa que el Ministerio de Sanidad sigue fomentando la inclusión de nuevos fármacos en la cartera de servicios del SNS y la agilidad en la toma de decisiones. Manteniendo generalmente estable el porcentaje de acuerdos positivos de financiación desde 2021, y viéndose ligeramente incrementado el porcentaje de acuerdos positivos tomados en una primera reunión de la CIPM (70% en 2025 frente a 54% - 68% entre 2021 y 2024).
- En línea con lo observado en desde el inicio del análisis en 2021, se puede concluir que la implementación de medidas de control del gasto asociadas a estos acuerdos se mantiene como requisito indispensable para la financiación, ya que todos los acuerdos positivos negociados en 2025 conllevaban al menos una de estas medidas.
- Asimismo, la implementación de restricciones en el acceso se ha mantenido estable respecto a los años anteriores, y sigue presentándose como una herramienta clave para contener el impacto presupuestario y garantizar el acceso a aquellos pacientes para los que existen resultados clínicos más robustos.
- Frente a 2024, se observa una notable disminución en la implementación de acuerdos especiales, pero las cifras de 2025 siguen la línea de los años previos. En 2025, se mantienen como opción principal los acuerdos puramente financieros apostando en su mayoría por el esquema de coste máximo por paciente y los acuerdos de precio volumen. Los acuerdos basados en resultados clínicos están siendo utilizados principalmente como una herramienta dirigida a productos altamente innovadores como las terapias avanzadas y génicas de administración única, debido a su alta carga administrativa. Esta disminución de acuerdos especiales negociados en el último año refuerza la preferencia del Ministerio por la negociación directa de un precio acorde con el valor demostrado por los productos innovadores, utilizando estos acuerdos especiales únicamente en aquellos casos en los que persistan incertidumbres clínicas además de presupuestarias.
- De acuerdo con este nuevo análisis, y como parte del proceso de preparación de la negociación de financiación de un medicamento, desde Simon-Kucher recomendamos que:
- Los laboratorios comercializadores evalúen los aspectos clave en torno al producto, entendiendo tanto las incertidumbres como las principales inquietudes que podría despertar en el Ministerio (ya sean clínicas y/o económicas) y preparen estrategias que permitan su mitigación.
- Además, debe definirse una estrategia de negociación clara, con concesiones evaluadas en profundidad, que permita al sistema asumir el coste de la innovación y que estén ligadas al beneficio clínico ofrecido por el fármaco.
- Asimismo, para casos de alto coste o de impacto presupuestario considerable, es muy recomendable que el laboratorio se prepare para discutir diferentes escenarios a lo largo de la negociación, incluso proponiendo algún tipo de acuerdo especial de financiación que permita al Ministerio de Sanidad reducir la incertidumbre económica (y clínica, si aplicara) del fármaco. Además, el tipo de acuerdo seleccionado debería aspirar a mitigar las incertidumbres mencionadas y estar alineado con las capacidades del sistema.
- Por último, cabe mencionar la modificación en curso de los procedimientos de evaluación de medicamentos, tanto a nivel europeo debido a la introducción de las evaluaciones clínicas conjuntas (JCA), como a nivel nacional, con la tramitación del Real Decreto de Evaluación de Tecnologías Sanitarias. La monitorización de estas nuevas normativas y su potencial impacto en las decisiones y condiciones de financiación será crucial para adaptarse a los cambios y optimizar el acceso a los medicamentos en el futuro.
Consideraciones para el análisis
(1) Acuerdos relativos a la inclusión o no inclusión en la prestación farmacéutica del Sistema Nacional de Salud (SNS) de medicamentos con nuevos principios activos o combinaciones (A.1) y de otros medicamentos (A.2). En lo referente al subapartado A.2; para este análisis sólo se han tenido en cuenta aquellos medicamentos que cambien sus condiciones de comercialización (por ejemplo, por pasar de estar no financiado a entrar en prestación o aquellas nuevas presentaciones que estén ligadas a una extensión de indicación). No se han contemplado primeros genéricos o biosimilares, se ha asumido que reciben las mismas condiciones de financiación que el medicamento original.
Acuerdos relativos a la inclusión o no inclusión en la prestación farmacéutica del SNS de nuevas indicaciones de medicamentos que ya están incluidos en la prestación farmacéutica del SNS.
(2) No se han estudiado las condiciones de financiación de aquellos medicamentos incluidos en el grupo "Alteraciones de la oferta". Es decir, la modificación de las condiciones de financiación y precio (precio al alza o la baja, condiciones de la prescripción y dispensación, exclusión de la prestación) de medicamentos incluidos en la prestación farmacéutica del SNS. Las vacunas y dispositivos médicos tampoco han sido objeto de estudio.
(3) El número de decisiones refiere únicamente a aquellos medicamentos seleccionados como objeto de este estudio: medicamentos con nuevos principios activos o combinaciones y nuevas indicaciones de medicamentos que ya están incluidos en la prestación farmacéutica del SNS.
Ana Mozetic es socia responsable de la división Healthcare & Life Sciences en España; Laura Sánchez-Calero, directora y Elena Aldareguia, manager en Simon-Kucher.

 Artículo de opinión de Ana Mozetic, Laura Sánchez-Calero y Elena Aldareguia (Simon-Kucher), sobre los acuerdos que han resultado de las negociaciones de financiación y precio de los medicamentos en España en 2025.
Artículo de opinión de Ana Mozetic, Laura Sánchez-Calero y Elena Aldareguia (Simon-Kucher), sobre los acuerdos que han resultado de las negociaciones de financiación y precio de los medicamentos en España en 2025.






 Lilisbeth Perestelo:
Lilisbeth Perestelo:  César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):