Con motivo del Día Mundial de las Enfermedades Raras, la Asociación Española de Laboratorios de Medicamentos Huérfanos y Ultrahuérfanos (Aelmhu) ha presentado su Informe Anual de Acceso de los Medicamentos Huérfanos en España que analiza la evolución y la situación actual de los medicamentos huérfanos en España.
El informe revela que en 2021 se ha producido una mejora en el acceso, en los tiempos de aprobación y en la financiación de medicamentos huérfanos, respecto al año anterior en el que se acusó el impacto de la pandemia de covid-19. En el último año se han incluido en el Sistema Nacional de Salud (SNS) 14 nuevos medicamentos huérfanos, frente a los 5 aprobados en 2020, con lo que el número actual de medicamentos huérfanos financiados es de 56.
A pesar de estos ratios, sólo el 50% de los medicamentos huérfanos que han llegado a nuestro país están financiados por el SNS, siendo una proporción muy similar a la que se ha mantenido en los últimos años (48% en 2019 y 46% en 2020). El tiempo medio para obtener dicha financiación ha sido de 24 meses, 11 menos que en 2020, si bien el promedio todavía se encuentra lejos de los 14 meses de 2019.
Según ha manifestado María José Sánchez Losada, presidenta de Aelmhu “los indicadores de acceso de los pacientes con enfermedades raras a sus tratamientos ha mejorado en el último año, como consecuencia del esfuerzo realizado por la Administración y por la flexibilidad mostrada por las compañías farmacéuticas, pero tenemos que recordar que esta mejoría sólo supone recuperar los retrasos acumulados durante la pandemia”.
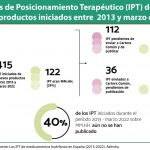
Los datos revelan que de los 55 tratamientos huérfanos pendientes de financiación, un 51% llevan esperando más de 3 años, evidenciando un retraso en el acceso para pacientes. Esta barrera puede incrementarse si la situación termina por desincentivar la llegada a España de la creciente innovación que se está produciendo en el ámbito de las enfermedades raras. Actualmente, 18 medicamentos húerfanos con autorización comercial no han llegado a España, de los cuales, un 61% tiene esta autorización desde hace más de un año.
El informe incluye por primera vez una visión específica de las terapias avanzadas, consideradas como los tratamientos con más perspectivas de futuro. En 2021, de los 14 medicamentos financiados por el SNS 2 han sido terapias avanzadas, y el tiempo medio para su aprobación ha sido de 21 meses. Las terapias avanzadas se encuentran, por tanto, en una situación similar al resto de medicamentos huérfanos, tanto en su financiación como en los tiempos de espera.
En este sentido, la presidenta reclama “avanzar hacia un nuevo modelo que permita a nuestro país un mejor acceso a la innovación en los tratamientos de enfermedades raras, especialmente teniendo en cuenta que la investigación farmacéutica se ha acelerado y va a ofrecer un mayor número de soluciones terapéuticas en los próximos años, capaces de mejorar la calidad de vida de los pacientes y la de sus familias“.
Para Aelmhu “es esencial revisar y mejorar el sistema actual para desarrollar un nuevo modelo que aporte mayor agilidad y claridad en los procesos, acortando los plazos y generando mayor certidumbre y consenso en las evaluaciones”. Estas medidas aumentarían el atractivo de España en este terreno, estimulando que el mayor número de terapias posible llegue a las personas afectadas por una enfermedad minoritaria.
Con este objetivo en el horizonte, la Asociación reitera su plena disposición para aportar su conocimiento y esfuerzo, convencida de que solo la unión de todos los agentes implicados en el proceso contribuirá a mejorar la calidad de vida de los pacientes con patologías poco frecuentes que, en la mayoría de los casos, carecen de tratamientos.












 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: