Las resoluciones favorables a las solicitudes para el tratamiento con medicamentos CAR-T realizadas por comunidades autónomas en las que no hay centros autorizados para su administración son sensiblemente inferiores a las de las regiones que sí los tienen. Así se desprende del análisis realizado por Diariofarma a partir de los datos del tercer informe de seguimiento del Plan para el abordaje de las terapias avanzadas en el SNS, fechado a junio de 2021.
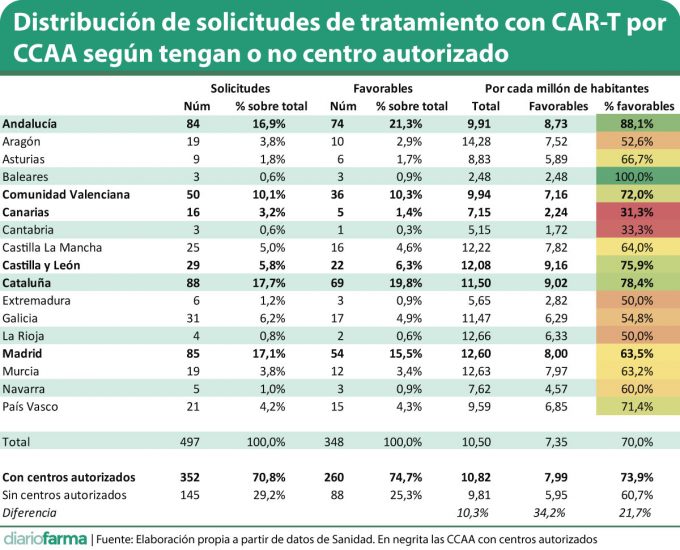
En concreto, de acuerdo con estos datos cerrados a marzo de 2021, las comunidades autónomas que tienen centros autorizados para la administración del tratamiento CAR-T, suman un total de 260 decisiones favorables por parte de los comités correspondientes a la petición de tratamiento. Esto supone 7,99 por cada millón de habitantes. Estas mismas respuestas positivas a las solicitudes de tratamiento en las comunidades autónomas sin centros autorizados se sitúan en 88, lo que supone 5,95 por cada millón de habitantes. Una diferencia muy importante del 34,2%.
A la vista de los datos también se observan diferencias en el éxito que tienen las solicitudes realizadas y la probabilidad de conseguir la autorización. Así, las comunidades autónomas con centros autorizados tienen una mayor probabilidad de conseguir que sus solicitudes sean aprobadas. Aquí, no obstante, la diferencia es relativamente baja (un 73,9% para las que tienen centro y un 60,7% para las que no), si bien podría deberse a la mayor experiencia de los primeros para seleccionar a los pacientes y preparar la documentación necesaria.
A este respecto también hay que reconocer que, aunque el ratio de resoluciones favorables a las solicitudes agrupado de comunidades con centros autorizados frente a las que no lo tienen es superior en las primeras, hay excepciones, como es el caso de Baleares, que ha confirmado sus tres solicitudes sin tener centros de administración, o Madrid, cuyo ratio de aceptación es inferior a la media nacional y a cuatro comunidades sin centros autorizados.
Como lo lógico es que la incidencia de las enfermedades tratables con CAR-T sea muy similar en las diferentes comunidades autónomas, solo cabe esperar que exista un factor exógeno, como es la proximidad a un centro autorizado, para explicar la importante diferencia observada. Pese a esta situación objetiva, que debería ser analizada con detenimiento por parte del Ministerio de Sanidad para ver si hay otros elementos que justifiquen la diferencia observada, el departamento de Carolina Darias no parece dispuesto a ampliar el número de centros autorizados para la administración de CAR-T ya que entre las conclusiones del informe de seguimiento solo se hace referencia a la presión asistencial como elemento clave para determinar la necesidad o no de más centros: “no se ha detectado sobrecarga asistencial, aun no estando todos los centros designados ya cualificados para tisagenlecleucel y axicabtagen ciloleucel y con la firma del contrato realizada”, señala. El informe pone de relevancia que en el tiempo estudiado no se disponía de todos los centros autorizados ya que algunos estaban en proceso de cualificación y firmas de contratos con las compañías fabricantes.
Tiempo para el tratamiento
Pese a la diferencia existente para la probabilidad de que se acepte o no el tratamiento en función de si la comunidad autónoma tiene o no centros autorizados, en lo que parece que no hay excesivas diferencias, y menos con impacto asistencial, es en los tiempos hasta la administración del tratamiento. En el proceso global desde la solicitud hasta la administración, la diferencia de sus medias es de 1,86 días, recoge el informe concluyendo que “la diferencia que existe entre un paciente que ha sido derivado y otro que se atiende en su propia comunidad es mínima”.
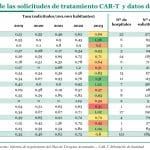
En lo que se refiere a la evolución de los procesos, cabe destacar la reducción generalizada de los plazos en cada una de las fases. Así, según el informe de junio de 2021, la aféresis se sitúa en una mediana de 14 días desde la solicitud y una media de 17,32±12,52 días, mejorando los 16,5 de mediana y 19,25±12,95 días registrados en el informe previo de diciembre de 2020.
Por su parte, los tiempos desde la aféresis al tratamiento han bajado en un día (de 48 a 47) en lo que se refiere tanto a la mediana como a la media. De este modo se ha pasado de tardar 67 (40-250) días como mediana y 70,24±23,11 de media a 64 (16-250) días de mediana y 67,24±21,76 días de media.
Solo un 61% de aceptados se tratan
De los datos incluidos en el informe también se puede extraer que solo en el 61% de las solicitudes que resultan favorables, los pacientes terminan recibiendo los tratamientos, lo que denota un importante margen de mejora, si bien esta cifra ha venido incrementándose según avanza el tiempo.
Diariofarma ha cogido los datos del informe respecto a solicitudes, número de aféresis y tratamientos mensuales y ha hecho un corte en diciembre de 2020 para evitar que la falta de datos o los tratamientos en curso pudieran desvirtuar estas conclusiones. Aún así, es cierto que las cifras están subestimadas debido al desfase temporal entre los tres pasos.
Así, en marzo de 2020, a un año de la puesta en marcha efectiva del Plan para el abordaje de las terapias avanzadas en el SNS, solo el 51% de las solicitudes autorizadas terminaban en administración del medicamento, mientras que en diciembre de 2020 ya se había alcanzado un 61%. Es decir, se ha pasado de que en marzo de 2020 el 64% de las aféresis terminen en tratamiento a un 78% nueve meses después.
Pese a esta cifra de evolución positiva, a lo largo del tiempo ha venido reduciéndose el número de aféresis que se realizan respecto de las autorizaciones. En marzo de 2020 el 80% de las solicitudes favorables llegaban a aféresis, mientras que a diciembre de 2020 esta cifra cayó hasta el 78%.
En concreto, el informe detalla que para linfoma B difuso de célula grande en 36 casos en los que se hizo la aféresis en los que no se ha realizado la administración dado que 27 fueron éxitus, dos por progresión de la enfermedad, dos por empeoramiento del estado del paciente, se produjeron tres fallos de producción, dos se anularon por decisión médica (un paciente obtuvo histología final de Linfoma Folicular y en otro caso se anuló porque el paciente sufría esquizofrenia). Por su parte en linfoma primario mediastínico no se administró en un paciente por fallecimiento y en leucemia linfoblástica aguda de células B no se realizó la administración del tratamiento en cinco pacientes debido a que dos casos fueron éxitus y en tres casos se produjo fallo de producción.
Efectividad de los tratamientos
Con respecto a los resultados finales de los tratamientos, de acuerdo con el informe de junio de 2021, solo se dispone del resultado de la administración de CAR-T en 117 pacientes, lo que supone menos de la mitad de los 244 tratamientos administrados.
Según estos datos, 48 pacientes fallecieron (27 de ellos a los 3 meses o antes, 21 desde los 3 a los 18 meses de la administración). La proporción de fallecimientos en los periodos más próximos a la administración del tratamiento hace presuponer que en muchos de ellos se ha retrasado la administración del tratamiento hasta que ya era demasiado tarde y no se han podido beneficiar en su totalidad de lo que ofrece la terapia. Lo mismo se puede decir de los 25 pacientes que progresaron precozmente ya que 20 de ellos lo hicieron a los 3 meses o antes, mientras que cinco evolucionaron entre los 3 y los 18 meses desde la administración.
En lo que se refiere a la respuesta completa, se alcanzó en 36 pacientes. De ellos, 27 a los 3 meses o antes, cuatro entre los 3 y los 12 meses y cinco a los 18 meses). Por otro lado, un paciente obtuvo respuesta completa con recuperación hematológica incompleta a los 3 meses o antes y siete pacientes obtuvieron respuesta parcial entre los 3 y los 18 meses.
Cabe señalar que en todo el periodo seguido ha habido 497 solicitudes: 402 con diagnóstico de linfoma (375 con linfoma B difuso de célula grande (LBDCG), se incluyen 18 reevaluaciones, y 27 de linfoma primario mediastínico (LPM), se incluye una reevaluación), y 95 con diagnóstico de leucemia linfoblástica aguda de células B (LLA-B).














 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: