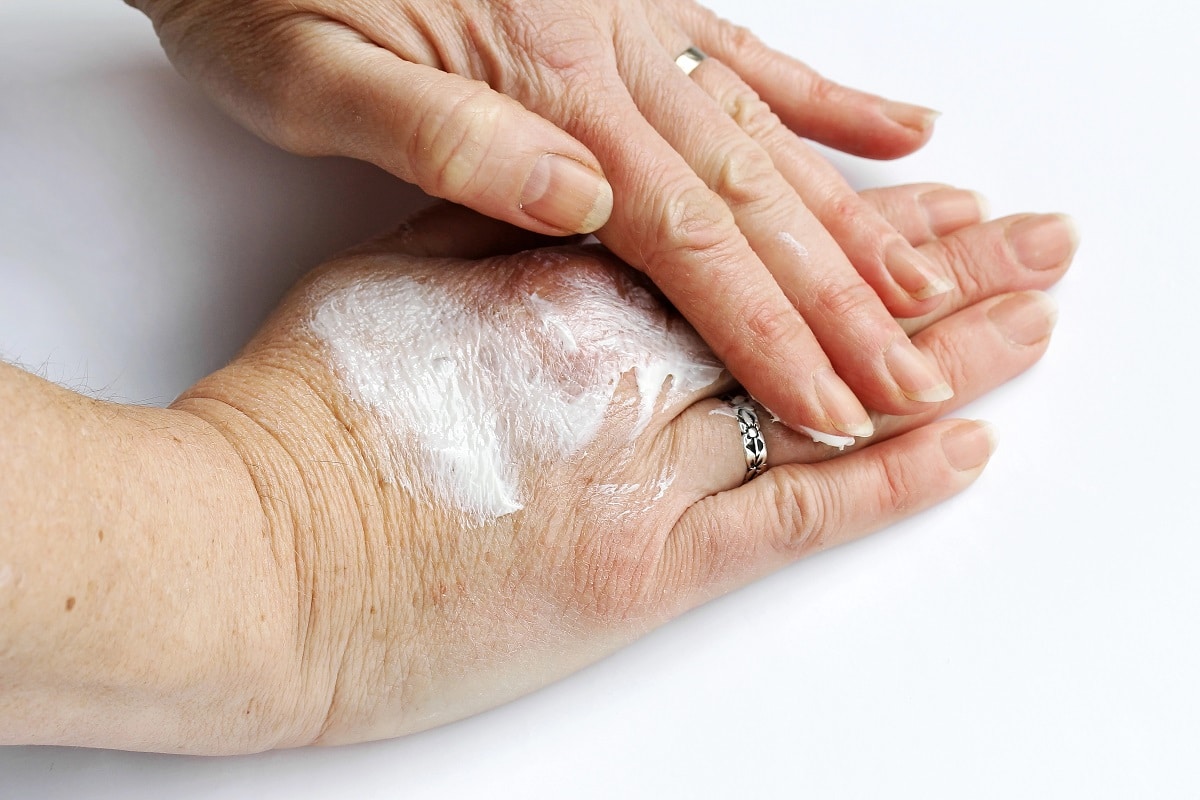
La pigmentación de la piel puede actuar como una "esponja" para algunos medicamentos, lo que podría influir en la velocidad con la que los medicamentos activos alcanzan sus objetivos previstos. Así lo aseguran los investigadores Sophie Zaaijer y Simon Groen, de la Universidad de Carolina Riverside, en un artículo de recientemente publicado en la revista Human Genomics.
Los investigadores sostienen que una proporción considerable de medicamentos y otros compuestos pueden unirse a los pigmentos de melanina en la piel, lo que genera diferencias en la biodisponibilidad y eficacia de estos medicamentos y otros compuestos en personas con distintos tonos de piel.
“Nuestro artículo de revisión concluye que la melanina, el pigmento responsable del color de la piel, muestra una sorprendente afinidad por ciertos compuestos farmacológicos”, dijo Simon Groen, profesor adjunto de biología de sistemas evolutivos en el Instituto de Biología Genómica Integrativa de la Universidad de California, Riverside, y coautor del artículo. “Las implicaciones de la melanina para la seguridad y la dosificación de los medicamentos se han pasado por alto en gran medida, lo que plantea preguntas alarmantes sobre la eficacia de la dosificación estándar, ya que las personas varían mucho en cuanto a tonos de piel”.
Según Groen y la coautora Sophie Zaaijer, consultora e investigadora afiliada a la UC Riverside que se especializa en diversidad, equidad e inclusión (DEI) en I+D preclínico y ensayos clínicos, las pautas actuales de la FDA para las pruebas de toxicidad no abordan adecuadamente el impacto de la pigmentación de la piel en las interacciones farmacológicas.

“Este descuido es particularmente preocupante dada la presión para realizar ensayos clínicos más diversos, como se describe en el Plan de Acción de Diversidad de la agencia”, dijo Zaaijer. “Pero las prácticas actuales de desarrollo de fármacos en las primeras etapas todavía se centran principalmente en las pruebas de fármacos en poblaciones blancas de ascendencia del norte de Europa”.
En un ejemplo, los investigadores encontraron evidencia de afinidad de la nicotina por los pigmentos de la piel, lo que podría afectar los hábitos de fumar en personas con una variedad de tonos de piel y plantear preguntas sobre la eficacia de los parches de nicotina adheridos a la piel para dejar de fumar.
“¿Estamos perjudicando inadvertidamente a los fumadores con tonos de piel más oscuros si recurren a estos parches en sus intentos de dejar de fumar?”, se pregutna Groen.
Groen y Zaaijer proponen utilizar un nuevo flujo de trabajo que involucra modelos de piel humana en 3D con diferentes niveles de pigmentación que podrían ofrecer a las compañías farmacéuticas un método eficiente para evaluar las propiedades de unión de los fármacos en diferentes tipos de piel.
“La pigmentación de la piel debe considerarse como un factor en las estimaciones de seguridad y dosificación”, dijo Zaaijer. “Estamos al borde de una era transformadora en la industria biomédica, donde adoptar la inclusividad ya no es solo una opción, sino una necesidad”.
Según los investigadores, la pigmentación de la piel es solo un ejemplo. Las variaciones genéticas entre los grupos minoritarios pueden dar lugar a respuestas a los medicamentos muy diferentes según las razas y etnias, lo que afecta hasta al 20% de todos los medicamentos, dijeron.
Los investigadores reconocen que las transformaciones que mejoran la inclusión (que abarcan la raza, la etnia, el sexo y la edad) exigen una revisión integral de todas las directrices de la FDA sobre los criterios de valoración clínicos para alinearlas con el Plan de Acción de Diversidad de la FDA.
“Es una tarea monumental, que requiere líneas de comunicación claras entre académicos, investigadores de la industria, médicos y reguladores”, dijo Zaaijer. “El futuro de la medicina depende de nuestra capacidad para conectar a estos equipos operativos actualmente aislados”.
Medicamentos inclusivos
Los investigadores señalan que se producirá un cambio hacia el desarrollo de medicamentos inclusivos, impulsado por una nueva ley, la Ley Ómnibus de Reforma de Alimentos y Medicamentos, estadounidense promulgada en 2022.
“La FDA publicó recientemente sus directrices preliminares”, dijo Zaaijer. “Una vez que estén listos, en unos meses, se exigirá que se tenga en cuenta la diversidad de pacientes en los ensayos clínicos y en la investigación y el desarrollo preclínicos. El siguiente paso es proporcionar orientación sobre qué variables farmacocinéticas se deben probar en los procesos de investigación y desarrollo de medicamentos en su búsqueda de medicamentos equitativos”.
Los investigadores esperan activar a la industria farmacéutica y al mundo académico para que comiencen a realizar evaluaciones experimentales sistemáticas en la investigación preclínica en relación con la pigmentación de la piel y la cinética de los fármacos.
También alientan a los pacientes, a sus grupos de apoyo y a los participantes de los ensayos clínicos a que hagan preguntas relacionadas con la eficacia y la seguridad de los fármacos según la ascendencia, como por ejemplo: "¿Se ha probado este fármaco para ver si es seguro para personas de diferentes orígenes ancestrales, incluido el mío?". Los médicos y los representantes farmacéuticos deberían poder proporcionar un documento fácil de entender que describa los resultados de las distintas pruebas, dijeron los investigadores.
"En términos de pruebas de perfil de riesgo, los fármacos se prueban con mayor frecuencia en uno o unos pocos modelos de células humanas que en su mayoría provienen de donantes de ascendencia del norte de Europa", dijo Zaaijer. "Luego, los fármacos se prueban en un modelo de roedores. Si estas pruebas tienen éxito, las compañías farmacéuticas impulsan el fármaco hasta los ensayos clínicos. Pero, ¿están preparados los medicamentos para administrarse a un grupo diverso de pacientes si antes no se han probado, por ejemplo, en modelos de células humanas de diferentes ascendencias? ¿Se tiraría desde un puente si sabe que las cuerdas no han sido probadas para su categoría de peso? Es poco probable. Entonces, ¿por qué esto es aceptable actualmente con los medicamentos?”.
Groen explicó que en diferentes antecedentes ancestrales ciertas variantes genéticas son más frecuentes. Esas variantes pueden afectar la forma en que se metaboliza un medicamento y cómo se comporta en un cuerpo, dijo.
“Si se tienen en cuenta los diferentes antecedentes ancestrales en las primeras etapas del descubrimiento de fármacos, entonces diversos grupos de personas pueden tener más confianza en el proceso de desarrollo de fármacos y participar en ensayos clínicos porque estarán mejor informados de los posibles riesgos asociados”, concluyó.
















 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: 