La accesibilidad a los nuevos medicamentos se va acelerando en nuestro país. De acuerdo con los datos que maneja el Ministerio de Sanidad, la decisión de financiación llegó, para los medicamentos autorizados en 2023, un total de 176 días antes que para los medicamentos autorizados en 2020. De este modo, se ha pasado de 519 días a 345 desde la autorización a la decisión de la Comisión Interministerial de Precios de los Medicamentos (CIPM), tal y como se recoge en el informe ‘Financiación de Medicamentos Innovadores en España’.
El Ministerio de Sanidad se ha adelantado a la publicación del Informe WAIT, que se espera inminente, y ha hecho público su propio informe que aborda los mismos aspectos que el elaborado por IQVIA para la Federación Europea de la Industria Farmacéutica (Efpia).
Para Sanidad, se trata de avanzar en transparencia, así como mostrar el trabajo y esfuerzo realizado. Así se destacó por el secretario de Estado de Sanidad, Javier Padilla, y el director general de Cartera Común de Servicios del SNS y Farmacia, César Hernández, que ofrecieron una rueda de prensa para presentar los datos principales del informe.
“Cumplimos el compromiso de hacer públicos datos que hasta ahora eran públicos, pero no publicados”, afirmó Javier Padilla, durante la presentación del informe. Tal y como quiso poner de manifiesto, con esta iniciativa, Sanidad pone fin a la “dependencia de informes elaborados por terceros” y establece las bases de una serie histórica propia que se completará próximamente con un cuadro de mandos de acceso libre. Según Padilla esto permitirá que cualquier interesado pueda replicar los análisis oficiales y realizar sus propios seguimientos. “Los datos, no solo deben ser públicos, también deben estar publicados y publicitados”, aseguró.
Mejora de las expectativas
Padilla también realizó una valoración general de los motivos por los que se ha producido esta mejora. Para él, podría deberse a una “mejora de las expectativas en lo relacionado a la financiación en nuestro país” observada por la industria, lo que le hace adelantar la solicitud del código nacional y, además, se está mejorando en la disponibilidad de medicamentos en España sobre el total de fármacos autorizados en Europa. Según los datos de Sanidad, esta cifra alcanza ya el 84%.
Por otro lado, el secretario general explicó que hay otro “elemento fundamental: el diálogo temprano”. Esto permite a las compañías “entender las necesidades de la Administración, la disponibilidad a pagar o los esquemas de financiación”. Igualmente, Padilla valoró el trabajo de todos los miembros de la CIPM y todos los profesionales que forman parte de la cadena. En este sentido, Hernández también destacó la labor de los funcionarios de la Dirección General que lidera y que hace posible que el trabajo se realice en menos tiempo.
Hernández puso de manifiesto la importancia del diálogo con las compañías para “manejar sus expectativas” y hacer que la negociación empieza “en el punto más cercano posible, siendo muy claros en qué es lo que se pide, qué es lo que estaríamos dispuestos a hacer y cómo trabajarlo”, explicó. De este modo, el objetivo de ese diálogo es reducir aún más los tiempos, para que las compañías presenten sus “mejores ofertas” lo antes posible y reduciendo el número de veces que pasa un medicamento por la CIPM. Para ello, el director general planteó la necesidad de establecer nexos de “confianza mutua” entre las compañías y el Ministerio para que ante una buena propuesta, se puede aprobar a la primera.
Reducción de plazos y mejora en disponibilidad
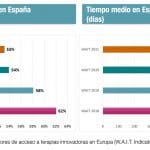
Entrando a valorar los datos del informe, cabe destacar que en el periodo 2020-2023 se ha producido también una mejora sustancial en la disponibilidad de la innovación. El porcentaje de medicamentos innovadores financiados ha pasado del 53% en 2020 al 75,9% en 2023, con un incremento relativo del 35,5%. “Esta tendencia positiva es diferencial en Europa”, destacó Padilla, en referencia al hecho de que países como Alemania, Francia, Italia o Reino Unido han disminuido su porcentaje de financiación, en contraposición con España, donde ha aumentado de forma sostenida desde 2020.
Además, los dirigentes del Ministerio destacaron que más de la mitad de estos medicamentos autorizados (52%) estuvieron disponibles antes de su financiación oficial, gracias al acceso mediante medicamentos en situaciones especiales (MSE), regulado por el Real Decreto 1015/2009. Esta vía permite acortar sustancialmente el tiempo real de acceso para los pacientes y, según el informe, si se tiene en cuenta este uso, los tiempos efectivos de disponibilidad se reducen hasta en un 56%.
Con esta información, se da respuesta a una de las quejas recurrentes del Ministerio respecto del informe WAIT, ya que, según indican, para otros países se toman los datos de acceso tempranos, pero para España no. Ese es uno de los motivos por los que Sanidad ha publicado su propio informe de plazos de acceso. En este sentido, Padilla explicó que ofrecieron a IQVIA los datos sobre MSE en nuestro país, para ser incorporados al informe, pero la respuesta obtenida no fue satisfactoria.
Respecto de la regulación de los MSE, tanto Padilla como Hernández, explicaron que se actualizará una vez que la ley de los Medicamentos esté vigente ya que es necesario distinguir claramente los usos compasivos de otras situaciones tras la autorización de los medicamentos. A este respecto, Hernández recordó que el anteproyecto de Ley ya recoge los accesos acelerado, provisional y condicional.



















 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: 