La Comisión Europea ha reconocido el sistema de información ‘Horizon Scanning’ de la Asociación Española de Medicamentos Biosimilares (BioSim) como referencia en el seguimiento de biosimilares en desarrollo en Europa. Así lo recoge el informe comunitario ‘Capacity building to support the uptake of biosimilars in a multistakeholder approach’, que identifica esta herramienta como la única fuente pública con datos detallados por principio activo.
El documento subraya que la información de acceso público sobre biosimilares en desarrollo sigue siendo limitada en el ámbito europeo y destaca que “la única fuente pública identificada que proporciona datos por principio activo sobre los biosimilares en desarrollo es el sistema de información mantenido por la asociación española de la industria de biosimilares (BioSim)”.
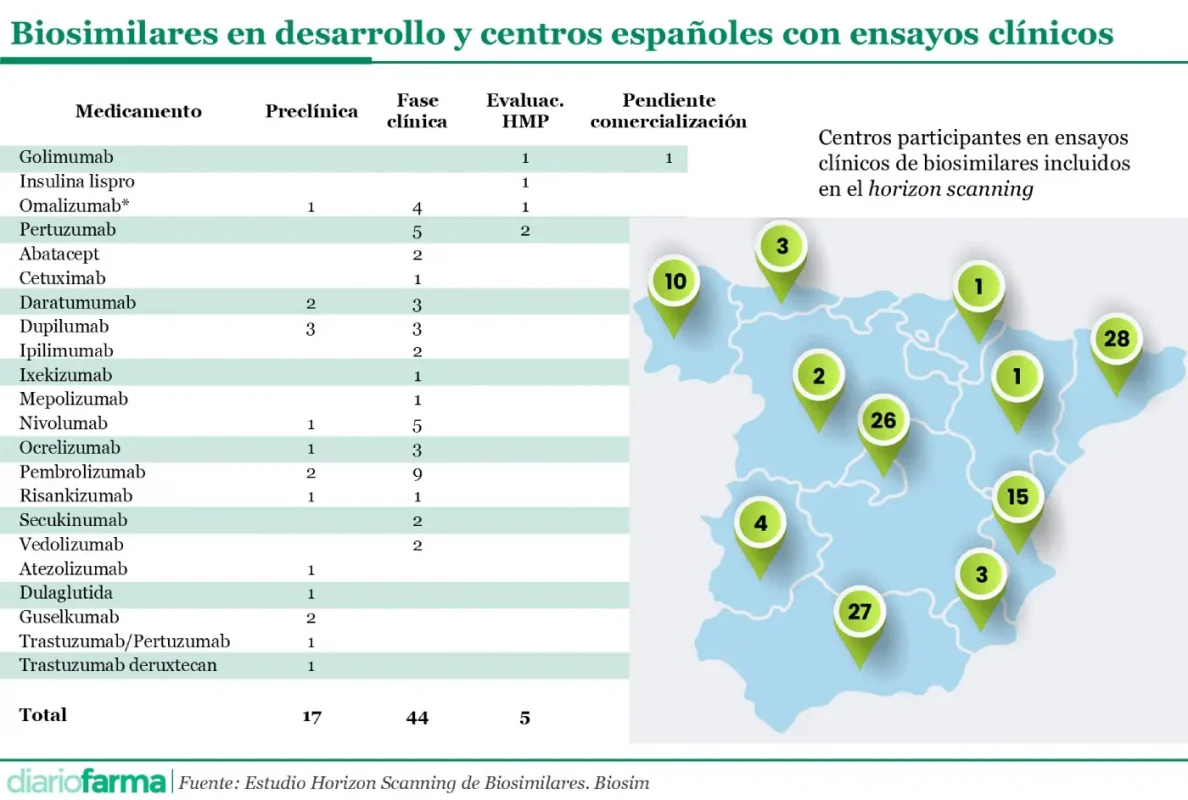
BioSim publicó recientemente la primera actualización de 2026 de su informe ‘Horizon Scanning’, concebido como una herramienta de apoyo a la planificación sanitaria y a la toma de decisiones informadas por parte de gestores y profesionales del sistema sanitario.
El presidente de BioSim, Joaquín Rodrigo, valoró esta mención como un respaldo al enfoque de transparencia y anticipación de la asociación. Señaló que el reconocimiento de la Comisión Europea refuerza el compromiso con la generación de conocimiento útil para preparar la llegada de la competencia biosimilar y optimizar recursos desde las primeras fases.
Cambios en el horizonte de biosimilares
La actualización de enero de 2026 refleja la evolución del mercado. Tras su lanzamiento comercial a finales de 2025, denosumab y aflibercept dejan de formar parte del informe, al tratarse de principios activos con varios biosimilares ya disponibles.
En paralelo, el documento incorpora seis nuevos principios activos que evidencian el avance hacia desarrollos biotecnológicos de mayor complejidad. En oncología, además del primer candidato en fase preclínica de atezolizumab, se incluyen también, en esta misma fase, un candidato de trastuzumab/pertuzumab y otro de trastuzumab deruxtecan, este último considerado el primer biosimilar de un anticuerpo monoclonal conjugado. Todos ellos están indicados para el tratamiento del cáncer de mama HER2+ o de otros tumores, según el caso.
Asimismo, se incorporan al seguimiento ixekizumab, risankizumab y guselkumab, con indicación en psoriasis.
Avances regulatorios y expectativas
El informe también destaca la evolución de los biosimilares de pertuzumab, que han avanzado posiciones respecto a la edición anterior. En la actualidad, existen dos candidatos en evaluación por la Agencia Europea del Medicamento (EMA), lo que los sitúa entre las posibles nuevas autorizaciones previstas para 2026.
La directora general de BioSim, Encarna Cruz, explicó que la entrada en el horizonte de candidatos como trastuzumab deruxtecan refleja la capacidad de la industria biosimilar para abordar terapias de alta complejidad técnica. Según señaló, este avance puede contribuir a aliviar el impacto presupuestario en áreas como la oncología y la inmunología, donde el gasto farmacéutico aumenta de forma sostenida por la llegada de innovaciones de alto coste.
Cruz subrayó también el compromiso del sector con la investigación y el desarrollo de nuevos biosimilares y su impacto directo en la mejora de la salud de los ciudadanos.
Participación española en ensayos clínicos
La actualización del ‘Horizon Scanning’ pone de relieve, además, la creciente implicación de centros españoles en el desarrollo clínico de biosimilares. En concreto, catorce hospitales se han incorporado a la investigación clínica de candidatos biosimilares de pembrolizumab, reforzando el papel de España como polo de atracción de ensayos clínicos en este ámbito.
Alcance del Horizon Scanning de BioSim
El ‘Horizon Scanning’ de BioSim ofrece una visión actualizada de los biosimilares en fases preclínicas, clínicas y de evaluación por la EMA. En el ámbito nacional, incluye también la fase de decisión de precio y financiación previa a la comercialización.
El informe incorpora una nota metodológica detallada que permite a los distintos agentes del sector, desde la administración hasta los profesionales clínicos, disponer de información precisa sobre los plazos estimados y los criterios utilizados para anticipar la llegada de estos medicamentos al Sistema Nacional de Salud.






 Lilisbeth Perestelo:
Lilisbeth Perestelo:  César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):