El Instituto Nacional de Gestión Sanitaria (Ingesa), dependiente del Ministerio de Sanidad, como órgano de contratación, ha formalizado el segundo Acuerdo Marco para el suministro de medicamentos biológicos con biosimilares para varias comunidades autónomas, centros del Ingesa en Ceuta y Melilla y el Ministerio de Defensa.
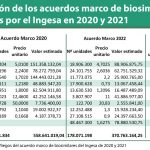
Este acuerdo marco supone la continuidad del primero y su actualización, ya que introduce nuevos lotes de acuerdo con la comercialización de nuevos medicamentos biosimilares. El primer acuerdo marco de esta naturaleza entró en vigor en el último trimestre de 2022 y ya ha dejado de estar vigente debido a la formalización del nuevo acuerdo. Su ahorro ha sido de más de 120 millones de euros para las administraciones públicas adheridas, segíun explica el instituto.
Este segundo acuerdo marco tiene un plazo de vigencia previsto de 24 meses, con la posibilidad de prórroga por 12 meses. Su valor estimado asciende a 410.940.221 euros y a él se han adherido diez comunidades autónomas (Aragón, Asturias, Cantabria, Castilla y León, Cataluña, Extremadura, La Rioja, Madrid, Murcia y Navarra), INGESA (que gestiona los servicios públicos de salud de Ceuta y Melilla) y el Ministerio de Defensa.
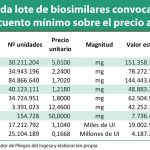
Mediante este acuerdo marco, el Ingea ha selecionado a los laboratorios farmacéuticos que suministrarán los distintos medicamentos biosimilares. Esta acción de compra centralizada para el Sistema Nacional de Salud supondrá un ahorro de 178 millones de euros para el conjunto de las administraciones adheridas.
En este acuerdo marco se incluyen diecisiete lotes. Entre ellos, los corresponde a inmunosupresores como Adalimumab, Etanercept e Infliximab, pertenecientes al subgrupo terapéutico L04AB (inhibidores del factor de necrosis tumoral alfa, indicados para el tratamiento de enfermedades autoinmunes como artritis, psoriasis y enfermedad de Crohn) y Anticuerpos monoclonales como Rituximab, Trastuzumab y Bevacizumab), del subgrupo terapéutico L01XC.
También quedan recogidas hormonas como la Somatropina, del subgrupo terapéutico H01A es la hormona de crecimiento indicada para el tratamiento a largo plazo en niños con baja talla debida a una secreción insuficiente de la hormona de crecimiento y para tratamiento de adultos deficitarios; agentes inmunomoduladores como Pegilgrastim y Filgrastim del subgrupo terapéutico L03AA (factores estimulantes de colonias, indicados para reducir la duración de la neutropenia en pacientes con tumores tratados con quimioterapia citotóxica); antianémicos como la Epoetina Alfa, perteneciente al subgrupo terapéutico B03XA, todos ellos eritropoyetinas de origen recombinante, indicados para el tratamiento de la anemia asociada a la insuficiencia renal crónica, a la quimioterapia por tumores sólidos, a la prevención de riesgos quirúrgicos y a la anemia en prematuros.
Otros fármacos incluidos son Tocilizumab y Ustekinumab, Inmunosupresores pertenecientes al subgrupo terapéutico L04AC (Inhibidores de la interleucina); Natalizumab, inmunosupresor perteneciente al subgrupo terapéutico L04AG (Anticuerpos monoclonales) para tratar la esclerosis múltiple, Eculizumab, inmunosupresor perteneciente a subgrupo terapéutico L04AJ (Inhibidores del sistema del complemento), para tratar las enfermedades de Hemoglobinuria paroxística nocturna y el Síndrome hemolítico urémico atípico y Ranibizumab, Agentes contra trastornos vasculares oculares, perteneciente a subgrupo terapéutico01LA (Agentes Antineovascularización) y que se utiliza en adultos para tratar varias enfermedades oculares que causan alteración de la visión, entre otros.














 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: